从全球范围来看,肺癌的发病率在各类恶性肿瘤中高居第 2 位,而其死亡率更是令人触目惊心,位列恶性肿瘤之首。仅仅在 2020 年这一年,就有约 180 万例患者被肺癌无情地夺走生命,这一庞大数字背后,是无数家庭的破碎以及社会医疗资源面临的巨大挑战。
在众多肿瘤分期系统中,TNM 分期脱颖而出,尤其是在包括肺癌在内的实体瘤领域,它的应用最为广泛。这一系统所构建的统一分期方法,其意义远超乎想象。一方面,它为全球各国的医学专家搭建起一座沟通无阻的桥梁,提供了通用的学术语言,使得国际间有关肿瘤诊疗的学术交流得以顺畅进行,不同地区的研究成果能够迅速共享、碰撞出创新的火花;另一方面,对于每一位肺癌患者个体而言,TNM 分期是医生判断疾病预后的得力助手,也是制定后续精准治疗决策的关键依据。医生依据 TNM 分期,能够清晰地洞察患者病情所处阶段,进而为患者量身定制最为适宜的治疗方案,从手术、放疗、化疗到新兴的靶向治疗、免疫治疗等,每一个决策都因 TNM 分期而有的放矢。
TNM 分期系统作为当下国际上应用最为广泛的肿瘤分期系统,已然成为临床上对恶性肿瘤进行分期的权威标准方法。 1968 年,具有里程碑意义的第 1 版《恶性肿瘤 TNM 分类法》手册重磅问世,为全球范围内恶性肿瘤患者的临床诊疗实践点亮了一盏明灯,提供了极具价值的参考依据。在 2023 年 9 月 11 日,于新加坡盛大召开的 2023 世界肺癌大会(WCLC)现场,来自日本的 Hisao Asamura 教授揭晓了肺癌 TNM(第九版)分期 的关键更新要点。此次备受瞩目的第九版 “国际肺癌 TNM 分期标准”,着重对 N 分期、M 分期进行了精细打磨与更新,毋庸置疑,它将为肺癌临床诊疗实践的进一步优化与细化注入强劲动力。
本次分期基于全新的数据库,涵盖2011—2019年间25个国家75个中心的124 581例肺癌患者的数据,在排除数据不完整的患者后,共纳入87 043例患者的资料,并基于此分析结果,对第八版肺癌TNM分期进行调整,更新成第九版肺癌TNM分期。此版中亚洲患者占比提升,中国患者占比增幅显著。第九版肺癌TNM分期将为肺癌诊治及预后评估提供更合理的参考依据。本文就IASLC第九版肺癌TNM分期标准的数据库更新、分期变化及其修订依据进行解读,为大家提供参考。
IASLC在2023年2月发布了第九版肺癌分期数据库。该数据库收集了2011 年—2019年期间来自25个国家和75 个中心的124 581 例肺癌患者的临床资料。其中亚洲64045 例(51.4%),欧洲30827例(24.7%),北美洲19608 例(15.7%),澳洲5704 例(4.6%),中南美洲4225例(3.4%),非洲及中东172例(0.1%)。排除不合格患者的临床资料后,纳入87043 例有效患者的临床资料用于分析,其中浸润性腺癌52069 例(59.8%),鳞状细胞癌15872例(18.2%),原位腺癌1 142例(1.3%),腺鳞癌1100例(1.3%),大细胞癌1057 例(1.2%),小细胞癌5530例(6.4%),大细胞神经内分泌癌689 例(0.8%)。
第九版肺癌分期数据库的数据来源分为两种形式,分别是经过预处理的批量数据集和保留原始数据的病历电子数据采集(electronic data capture, EDC)系统。EDC系统支持投稿者在线提交及检索自身研究数据。该系统含有T分期、N分期及M分期的判定要素,以及在临床分期或病理分期中分类的具体理由。相比批量数据集,EDC系统在实时性、准确性、可追溯性及灵活性等诸多方面具有显著优势,更适合用于临床研究数据的采集与传输。然而,由于传统习惯、成本考虑及法规要求等多重因素,第九版肺癌分期数据库中EDC所占比例仅为18.9%(23548/124 581),大部分数据仍以批量数据集形式提交。四川大学华西医院作为国内重要的数据贡献方,共提供8010例患者的数据,占总数据的6.4%(8 010/124581),且全部为EDC数据,占数据库全部EDC病例的34.0%(8010/23548)。
2.1 T分期
T分期无改动。尽管第九版T分期的定义与前一版保持一致,但特别值得注意的是,SPFC就T3分期的不同亚型(侵犯胸壁的T3 与其他类型的T3)在预后方面的差异提出了深入的探讨。研究发现,在病理分期中,pT3-侵犯胸壁组的患者预后显著差于pT3-其他类型组,甚至接近于pT4的预后情况。然而,这一预后差异在临床分期中并未得到体现,即cT3-侵犯胸壁组与cT3-其他类型组的患者在预后上并无明显差别。考虑到T3 分期在不同情境下(病理与临床)的预后差异性,第九版分期系统最终决定将侵犯胸壁或壁层胸膜的情况仍归类为T3,而并未升级至T4。
2.2 N分期
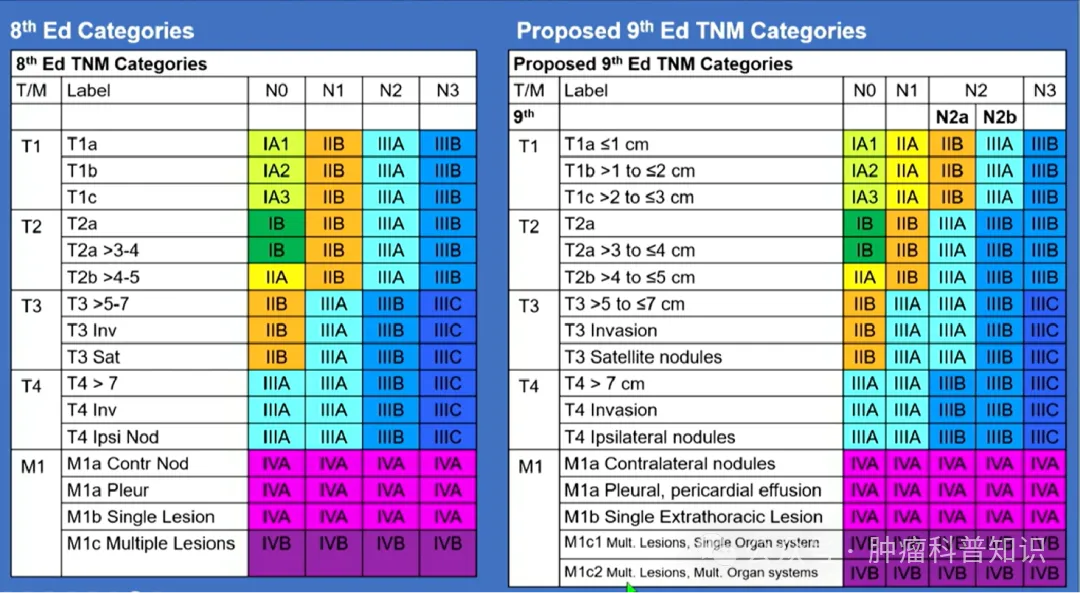
新版N分期将原N2淋巴结转移细分为N2a(单站转移)及N2b(多站转移)。第九版N 分期基于对大规模临床数据的分析(包括45032例临床N分期和35009 例病理N分期)将N2 细分为N2a(单站转移)及N2b(多站转移)。在N 分期的亚组分析中,研究者运用Kaplan-Meier生存分析法,对不同亚组分类间的5年生存率进行了深入评估。若所观察到的生存率差异小于5%,则该亚组分类被视为在临床上无显著意义。为了更精确地揭示这些差异,研究者进一步采用了多变量Cox比例风险生存模型来确定各亚组的风险比。在N分期的亚组分析中,研究者对N1a(单站N1)、N1b(多站N1)、N2a1(不涉及N1 的单站N2 或跳跃性转移)、N2a2(涉及N1 的单站N2)以及N2b(多站N2)进行了详尽的探索性分析。研究结果显示,各个N1亚类之间的5 年生存率估计值差异以及N1 亚类与N2a1 之间的差异均较小,差异无统计学意义,并且在临床和病理分期上也未呈现出一致性。相比之下,N2亚组之间的差异有统计学意义。基于上述分析结果,第九版N分期决定维持对N0、N1、N3 的原有描述,仅对N2 进行细分,将其划分为N2a和N2b两个子类别。这一调整旨在更准确地反映不同N2 亚组之间的生存率差异,并为临床实践提供更精准的分期指导。
临床实践中,N分期对治疗方案的选择具有重要影响。单站与多站、融合与非融合、可切除与不可切除等因素都会直接影响治疗策略制定。过去,由于对此类患者划分不够精细,N2 患者的治疗模式存在混乱,包括诱导治疗后手术、根治性同步放化疗以及直接按晚期患者治疗等不同方法。新的TNM分期将单站N2患者单独分类,为临床医生提供了更为明确的指导,有助于实现局部晚期患者的细分和个体化治疗。
2.3 M分期
将原M1c(胸腔外多转移灶)细分为M1c1(胸腔外的多转移灶在同一器官)和M1c2(胸腔外的多转移灶在不同器官)。自2007 年IASLC首次发布第七版M分期以来,M分期的修订重点在于深入探讨胸腔外转移情况。2015 年发布的第八版将第七版中的M1b(胸腔外转移)细分为M1b(胸腔外单转移灶)与M1c(胸腔外多转移灶)。第九版将M1c(胸腔外多转移灶)进一步细分为M1c1(胸腔外的多转移灶在同一器官)和M1c2(胸腔外的多转移灶在不同器官)。在M分期亚组分析中,研究人员运用Kaplan-Meier生存分析法及多变量Cox比例风险生存模型探讨各M分期细分是否具有临床意义。结果显示,胸腔外多转移灶在同一器官(M1c1)的肿瘤患者生存结果[ 中位生存期1.0(0.9~1.0)年]介于胸腔外单转移灶(M1b)的肿瘤患者[ 中位生存期1.2(1.1~1.3)年]与胸腔外多转移灶在不同器官(M1c2)的肿瘤患者[ 中位生存期 0.6(0.6~0.7)年]之间,因此对M1c的细分有临床意义。
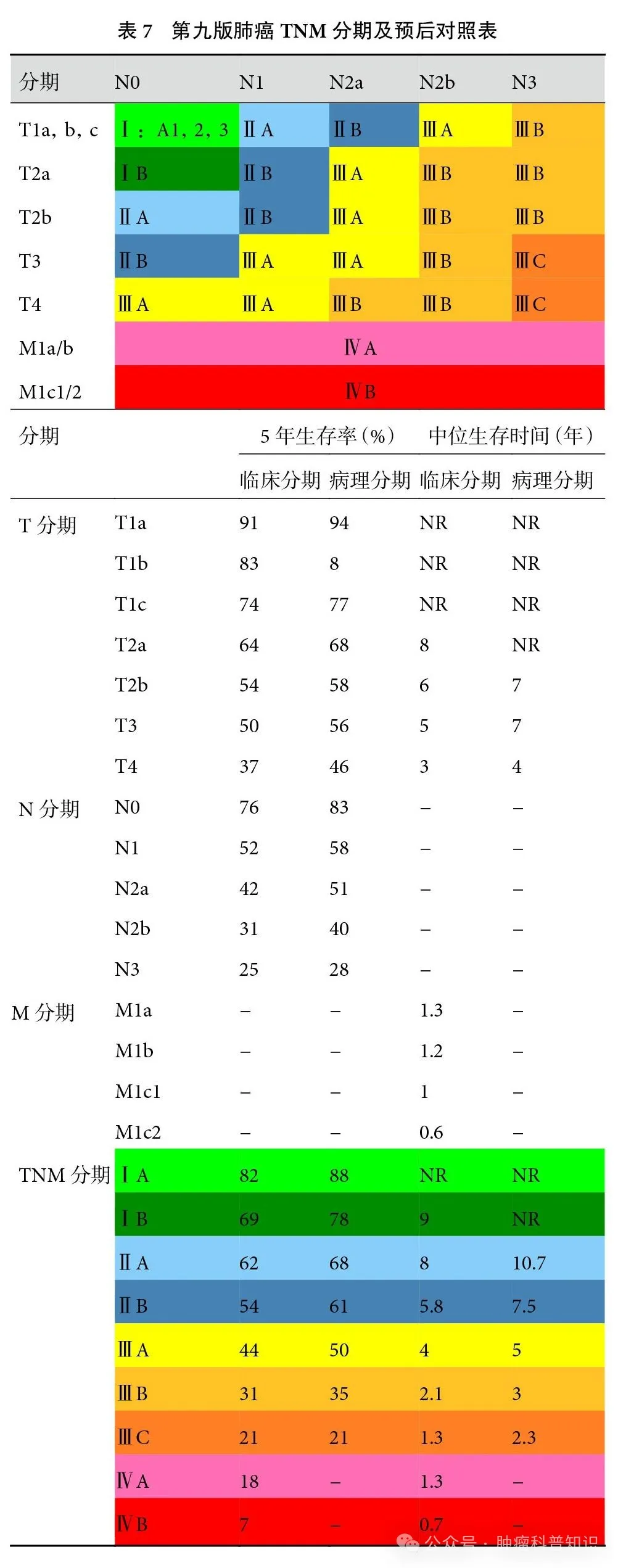
经过第九版N分期的调整,第九版TNM分期亦作相应变更。本次更新将T1N1M0 的预后由 ⅡB降为ⅡA。N2 细分为N2a和N2b后其对应关系做了如下调整:T1N2aM0归为ⅡB 期;T2a~3N2aM0及T1N2bM0 归为ⅢA期;T4N2aM0及T2a~4N2bM0 归为ⅢB期,其余分期不变。
TNM分期,是一种帮助医生了解患者病情发展到何种阶段的工具,正确使用可以对生存期做个预测,指导我们采取合适的方式尽快治疗,可以帮助分辨当前方案是否属于过度治疗。其对患者个体分期的评估以及预后的判断均具有重要意义。